1
堀本政夫ほか:応用薬理. 1991;42(2):167-176
2
Naito T,et al.:J Hum Lact. 2015;31(2):301-306
3
桑島巌ほか:Geriatric Medicine. 1991;29(6):899-902
4
Laine K,et al.:Br J Clin Pharmacol. 1997;43(1):29-33
5
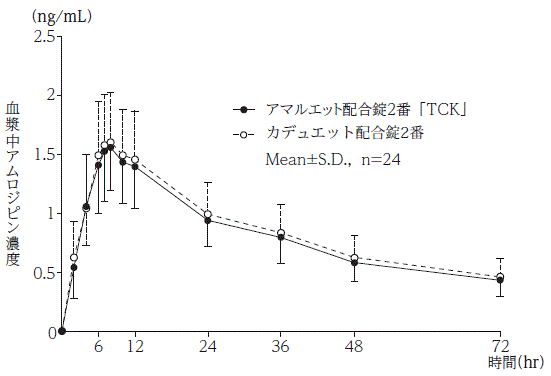
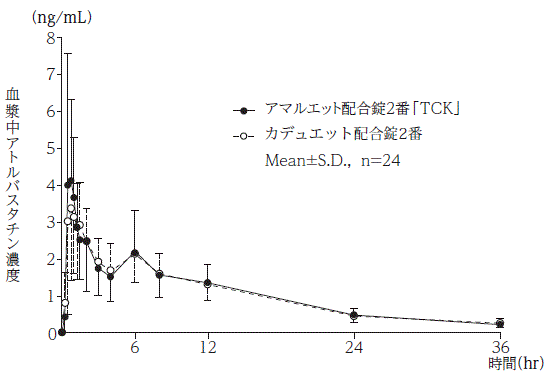
社内資料:生物学的同等性試験(配合錠2番)
6
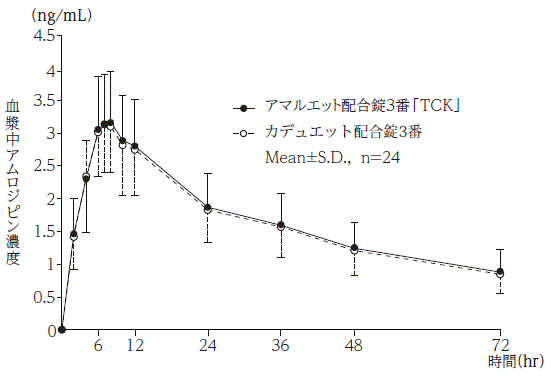
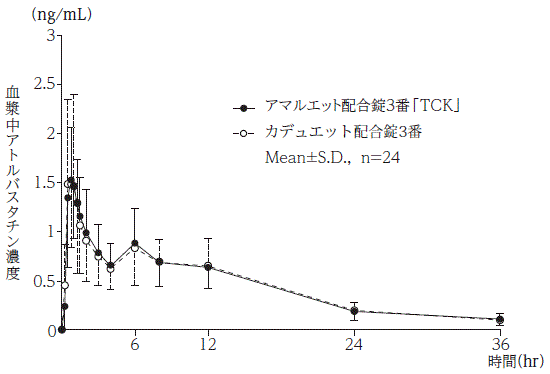
社内資料:生物学的同等性試験(配合錠3番)
7
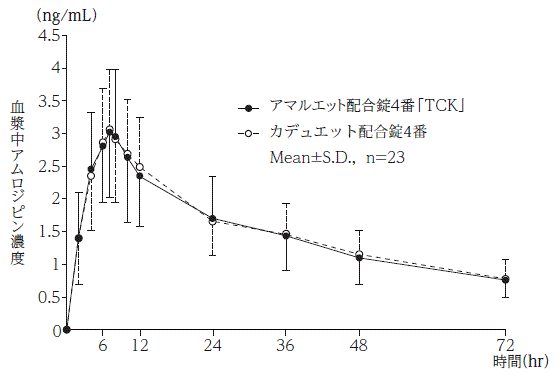
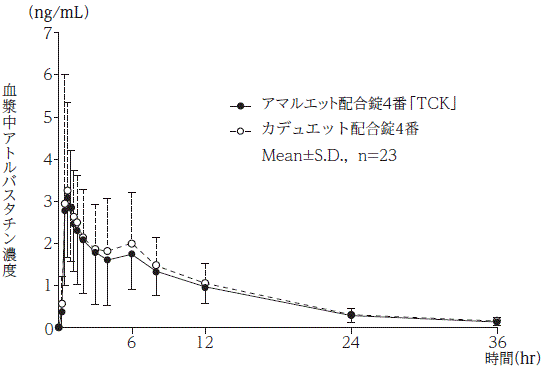
社内資料:生物学的同等性試験(配合錠4番)
8
足立幸彦ほか:薬理と治療. 1991;19(7):2923-2932
9
肝機能障害例における検討(リピトール錠:2000年3月10日承認、申請資料概要ヘ.3.(6).5))
10
大石紫満子ほか:薬理と治療. 1998;26(8):1295-1305
11
社内資料:生物学的同等性試験(配合錠1番)
12
Fujiwara, T. et al.:J Hum Hypertens. 2009;23(8):521-529
13
アムロジピン5mgで効果不十分な患者に対するアムロジピン10mgの長期投与試験(ノルバスク錠・OD錠、アムロジン錠・OD錠:2009年2月23日承認、審査報告書)
14
第十八改正 日本薬局方解説書. 廣川書店. 2021:C306-C311.
15
山中教造ほか:日本薬理学雑誌. 1991;97(3):167-178
16
作用機序(リピトール錠:2000年3月10日承認、申請資料概要ホ.1.8)