1
阿部真也 他:周産期医学.2017;47(10):1353-1355
2
齊藤大祐 他:鹿児島産科婦人科学会雑誌.2021;29:49-54
3
水山和之 他:医学と薬学.2009;62(2):279-295
胆汁・腎排泄型ACE阻害剤
1錠 39.5円
有効成分 | 1錠中 |
|---|---|
有効成分 | 日局 テモカプリル塩酸塩 1mg |
添加剤 | 乳糖水和物、ヒプロメロース、カルメロース、ショ糖脂肪酸エステル |
有効成分 | 1錠中 |
|---|---|
有効成分 | 日局 テモカプリル塩酸塩 2mg |
添加剤 | 乳糖水和物、ヒプロメロース、カルメロース、ショ糖脂肪酸エステル |
有効成分 | 1錠中 |
|---|---|
有効成分 | 日局 テモカプリル塩酸塩 4mg |
添加剤 | 乳糖水和物、ヒプロメロース、カルメロース、ショ糖脂肪酸エステル |
| 剤形 | 割線入りの錠剤 |
|---|---|
| 色調 | 白色~淡黄白色 |
| 外形 | 表面  裏面  側面  |
| 大きさ | 大きさ(直径) 5.0mm 大きさ(厚さ) 2.3mm |
| 質量 | 60mg |
| 識別コード | Tw521 |
| 剤形 | 割線入りの錠剤 |
|---|---|
| 色調 | 白色~淡黄白色 |
| 外形 | 表面  裏面  側面  |
| 大きさ | 大きさ(直径) 7.0mm 大きさ(厚さ) 2.4mm |
| 質量 | 120mg |
| 識別コード | Tw522 |
| 剤形 | 割線入りの錠剤 |
|---|---|
| 色調 | 白色~淡黄白色 |
| 外形 | 表面  裏面  側面  |
| 大きさ | 大きさ(直径) 8.5mm 大きさ(厚さ) 3.2mm |
| 質量 | 240mg |
| 識別コード | Tw523 |
| 薬剤名等 | 臨床症状・措置方法 | 機序・危険因子 |
|---|---|---|
デキストラン硫酸固定化セルロース、トリプトファン固定化ポリビニルアルコール又はポリエチレンテレフタレートを用いた吸着器によるアフェレーシスの施行 リポソーバーⓇ、イムソーバTRⓇ、セルソーバⓇ | ショックを起こすおそれがある。 | 陰性に荷電したデキストラン硫酸固定化セルロース、トリプトファン固定化ポリビニルアルコール又はポリエチレンテレフタレートによりブラジキニンの産生が刺激される。さらに本剤が、ブラジキニンの代謝を抑制するため、ブラジキニンの血中濃度が上昇する。 |
アクリロニトリルメタリルスルホン酸ナトリウム膜(AN69Ⓡ)を用いた透析 | アナフィラキシーを発現することがある。 | 陰性に荷電したAN69Ⓡ膜によりブラジキニンの産生が刺激される。さらに本剤が、ブラジキニンの代謝を抑制するため、ブラジキニンの血中濃度が上昇する。 |
アリスキレンフマル酸塩 ラジレス (糖尿病患者に使用する場合。ただし、他の降圧治療を行ってもなお血圧のコントロールが著しく不良の患者を除く。) | 非致死性脳卒中、腎機能障害、高カリウム血症及び低血圧のリスク増加が報告されている。 | レニン-アンジオテンシン系阻害作用が増強される可能性がある。 |
アンジオテンシン受容体ネプリライシン阻害薬(ARNI) サクビトリルバルサルタンナトリウム水和物 (エンレスト) | 血管浮腫があらわれるおそれがある。本剤投与終了後にARNIを投与する場合は、本剤の最終投与から36時間後までは投与しないこと。また、ARNIが投与されている場合は、少なくとも本剤投与開始36時間前に中止すること。 | 併用により相加的にブラジキニンの分解が抑制され、ブラジキニンの血中濃度が上昇する可能性がある。 |
| 薬剤名等 | 臨床症状・措置方法 | 機序・危険因子 |
|---|---|---|
カリウム保持性利尿剤 スピロノラクトン、トリアムテレン等 カリウム補給剤 塩化カリウム等 | 血清カリウム値が上昇するおそれがある。 | 機序:本剤はアンジオテンシンⅡ産生を抑制し、アルドステロンの分泌を低下させるため、カリウム排泄を減少させる。 危険因子:腎機能障害のある患者 |
利尿降圧剤 トリクロルメチアジド、ヒドロクロロチアジド等 | 本剤初回投与後、一過性の急激な血圧低下を起こすおそれがあるので、低用量から投与を開始すること。増量する場合は患者の状態を十分に観察しながら徐々に行うこと。 | 利尿降圧剤によるナトリウム排泄によって、レニン-アンジオテンシン系が亢進されているため、本剤によりアンジオテンシンⅡの産生が抑制されると、降圧作用が増強されると考えられている。なお、最近利尿降圧剤投与を開始した患者では特に注意すること。 |
リチウム製剤 炭酸リチウム | 他のアンジオテンシン変換酵素阻害剤(カプトプリル、エナラプリルマレイン酸塩、リシノプリル水和物)との併用により、リチウム中毒を起こすことが報告されている。 | 明確な機序は不明であるが、ナトリウムイオン不足はリチウムイオンの貯留を促進するといわれているため、本剤がナトリウム排泄を促進することにより起こると考えられる。 |
ニトログリセリン | 降圧作用が増強されるおそれがある。 | 両剤の降圧作用による。 |
アリスキレンフマル酸塩 | 腎機能障害、高カリウム血症及び低血圧を起こすおそれがある。 eGFRが60mL/min/1.73m2未満の腎機能障害のある患者へのアリスキレンフマル酸塩との併用については、治療上やむを得ないと判断される場合を除き避けること。 | レニン-アンジオテンシン系阻害作用が増強される可能性がある。 |
アンジオテンシンⅡ受容体拮抗剤 | 腎機能障害、高カリウム血症及び低血圧を起こすおそれがある。 | レニン-アンジオテンシン系阻害作用が増強される可能性がある。 |
非ステロイド性消炎鎮痛剤 | 降圧作用が減弱するおそれがある。 | 非ステロイド性消炎鎮痛剤は、血管拡張作用を有するプロスタグランジンの合成阻害作用により、本剤の降圧作用を減弱させる可能性がある。 |
非ステロイド性消炎鎮痛剤 | 腎機能を悪化させるおそれがある。 | プロスタグランジンの合成阻害作用により、腎血流量が低下するためと考えられる。 |
カリジノゲナーゼ製剤 | 過度の血圧低下が引き起こされる可能性がある。 | 血管平滑筋の弛緩が増強される可能性がある。 |
0.5%以上 | 0.1~0.5%未満 | 頻度不明 | |
|---|---|---|---|
過敏症 | 発疹、そう痒 | 蕁麻疹 | |
血液 | 白血球減少、好酸球増多 | 貧血、血小板減少 | |
精神神経系 | めまい、頭痛・頭重 | 眠気 | |
消化器 | 胃部不快感 | 嘔気、食欲不振、下痢 | 嘔吐、腹痛 |
肝臓 | AST上昇、ALT上昇 | ALP上昇、LDH上昇 | γ-GTP上昇、肝機能異常 |
循環器 | 動悸、低血圧 | ||
腎臓 | BUN上昇、血清クレアチニン上昇 | ||
その他 | 咳嗽(4.5%)注)、CK上昇 | 血清カリウム上昇、口渇、抗核抗体の陽性例 | 低血糖、嗄声、胸部不快感、咽頭不快感、顔面潮紅、倦怠感、味覚異常、浮腫 |
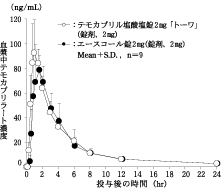
判定パラメータ | 参考パラメータ | |||
AUC24 (ng・hr/mL) | Cmax (ng/mL) | Tmax (hr) | T1/2 (hr) | |
テモカプリル塩酸塩錠 2mg「トーワ」 | 391.2±49.9 | 98.074±17.803 | 1.000±0.217 | 7.66±3.22 |
エースコール錠2mg | 371.7±85.8 | 85.508±14.435 | 1.333±0.433 | 8.29±1.80 |
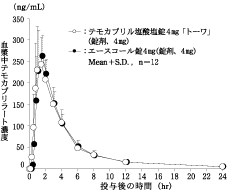
判定パラメータ | 参考パラメータ | |||
AUC24 (ng・hr/mL) | Cmax (ng/mL) | Tmax (hr) | T1/2 (hr) | |
テモカプリル塩酸塩錠 4mg「トーワ」 | 1096±244 | 216.263±76.195 | 1.292±0.582 | 6.566±0.500 |
エースコール錠4mg | 1100±216 | 277.903±60.984 | 1.417±0.289 | 6.614±0.493 |
 0120-108-932 FAX 06-7177-7379
0120-108-932 FAX 06-7177-7379