作成又は改訂年月
**
2024年1月改訂
(第8版)
*
2011年4月改訂
日本標準商品分類番号
薬効分類名
承認等
販売名
ダルテパリンNa静注5千単位/5mL「HK」
販売名コード
承認・許可番号
薬価基準収載年月
販売開始年月
貯法・使用期限等
貯法
室温保存
使用期限
外箱、容器に表示の使用期限内に使用すること。
規制区分
生物由来製品
処方箋医薬品注)
注)注意−医師等の処方箋により使用すること
組成
本剤は1瓶(5mL)中にダルテパリンナトリウム(ブタの小腸粘膜由来)を5,000低分子ヘパリン国際単位(抗第Xa因子活性)含有する。
添加物として等張化剤を含有する。
性状
組成及び性状の表
| pH | 5.0〜7.5 |
| 浸透圧比 | 1.0〜1.1(生理食塩液に対する比) |
一般的名称
禁忌
妊婦又は妊娠している可能性のある婦人
[「妊婦、産婦、授乳婦等への投与」の項参照]
原則禁忌
高度な出血症状を有する患者(汎発性血管内血液凝固症(DIC)を除く)
[症状が悪化するおそれがある。]
**ヘパリン起因性血小板減少症(HIT:heparin-induced thrombocytopenia)の既往歴のある患者
[HITがあらわれることがあるので、投与が必要な場合は、本剤投与後は血小板数を測定すること。](「その他の注意」の項参照)
本剤の成分又はヘパリン、他の低分子量ヘパリンに対し過敏症の既往歴のある患者
重篤な肝障害又はその既往歴のある患者
[血中濃度が上昇するおそれがある。]
効能又は効果
効能又は効果/用法及び用量
血液体外循環時の灌流血液の凝固防止(血液透析)
汎発性血管内血液凝固症(DIC)
用法及び用量
血液体外循環時の灌流血液の凝固防止(血液透析)
本剤を直接又は生理食塩液により希釈し投与する。
出血性病変又は出血傾向を有しない患者の場合
通常、成人には体外循環開始時、ダルテパリンナトリウムとして15〜20国際単位/kgを回路内に単回投与し、体外循環開始後は毎時7.5〜10国際単位/kgを抗凝固薬注入ラインより持続注入する。
出血性病変又は出血傾向を有する患者の場合
通常、成人には体外循環開始時、ダルテパリンナトリウムとして10〜15国際単位/kgを回路内に単回投与し、体外循環開始後は毎時7.5国際単位/kgを抗凝固薬注入ラインより持続注入する。
汎発性血管内血液凝固症(DIC)
通常、成人にはダルテパリンナトリウムとして1日量75国際単位/kgを24時間かけて静脈内に持続投与する。
なお、症状に応じ適宜増減する。
使用上の注意
重要な基本的注意
本剤の使用にあたっては、観察を十分に行い、出血の悪化がみられた場合には減量又は投与を中止すること。
脊椎・硬膜外麻酔あるいは腰椎穿刺等との併用により、穿刺部位に血腫が生じ、神経の圧迫による麻痺があらわれるおそれがある。
併用する場合には神経障害の徴候及び症状について十分注意し、異常が認められた場合には直ちに適切な処置を行うこと。
本剤の抗凝固作用を急速に中和する必要のある場合にはプロタミンを投与する。プロタミン1mgは本剤の100国際単位の効果を抑制する。
相互作用
他の薬剤との相互作用は、可能なすべての組合せについて検討されているわけではない。抗凝固療法施行中に新たに他剤を併用したり、休薬する場合には、凝固能の変動に注意すること。
併用注意
| 薬剤名等 | 臨床症状・措置方法 | 機序・危険因子 |
|---|
| 抗凝血剤(ヘパリンナトリウム、ワルファリン等) | 出血傾向が増強するおそれがある。 | 相加的に抗凝血作用が増強される。 |
|---|
| 血小板凝集抑制作用を有する薬剤(アスピリン、ジピリダモール等) | 出血傾向が増強するおそれがある。 | 血小板凝集抑制作用を有するため、抗凝血作用が増強される。 |
|---|
| *非ステロイド性消炎鎮痛薬(イブプロフェン等) | 出血傾向が増強するおそれがある。 | 血小板凝集抑制作用を有するため、抗凝血作用が増強される。
(特に腎不全のある患者) |
|---|
| 血栓溶解剤(ウロキナーゼ、t-PA製剤等) | 出血傾向が増強するおそれがある。 | 血栓溶解作用と、本剤の抗凝血作用の相加的作用による。 |
|---|
テトラサイクリン系抗生物質
強心配糖体(ジギタリス製剤) | 本剤の作用が減弱するおそれがある。 | 機序不明 |
|---|
副作用
副作用等発現状況の概要
本剤は使用成績調査等の副作用発現頻度が明確となる調査を実施していない。
重大な副作用
ショック・アナフィラキシー様症状
(頻度不明)
ショックが起こることがある。呼吸困難、浮腫等のアナフィラキシー様症状を伴うことがあるので、観察を十分に行い、異常が認められた場合には投与を中止し、血圧の維持、体液の補充管理、気道の確保等の適切な処置を行うこと。
出血
(頻度不明)
頭蓋内出血、消化管出血、後腹膜出血等の重篤な出血があらわれることがあるので、観察を十分に行い、出血又は出血の悪化等異常が認められた場合には投与を中止するなど適切な処置を行うこと。血液凝固能が著しく低下し、抗凝血作用を急速に中和する場合は、プロタミン硫酸塩を投与すること。
血小板減少
(頻度不明)
血小板減少があらわれることがあるので血小板数を測定し、著明な減少が認められた場合には投与を中止すること。
血栓症
(頻度不明)
著明な血小板減少とそれに伴う血栓症の発現が報告されている。ヘパリン起因性血小板減少症(HIT)の場合は、著明な血小板減少と脳梗塞、肺塞栓症、深部静脈血栓症等の血栓症やシャント閉塞、回路内閉塞を伴う。本剤投与後は血小板数を測定し、著明な減少や血栓症を疑わせる異常が認められた場合には投与を中止し、適切な処置を行うこと。
その他の副作用
次のような症状があらわれた場合には、必要に応じ、減量、投与中止等の適切な処置を行うこと。
過敏症注1)
頻度不明
そう痒感、発熱、発疹
肝臓
頻度不明
ALT(GPT)、AST(GOT)、Al-Pの上昇
消化器
頻度不明
嘔気、食欲不振
皮膚
頻度不明
脱毛
*その他
頻度不明
骨粗鬆症注2)
注1)このような症状があらわれた場合には投与を中止すること。
*注2)類薬(ヘパリン等)の長期投与で報告がある。
高齢者への投与
一般に高齢者では生理機能が低下しているので慎重に投与すること。
妊婦、産婦、授乳婦等への投与
妊婦
妊婦又は妊娠している可能性のある婦人には投与しないこと。
[妊娠中の投与に関する安全性は確立していない。]
授乳婦
投与中は授乳を避けさせること。
[動物実験(ラット)で、乳汁中へ移行することが確認されている。]
小児等への投与
低出生体重児、新生児、乳児、幼児又は小児に対する安全性は確立していない(低出生体重児、新生児、乳児又は幼児に対しては使用経験がない。小児には使用経験が少ない。)。
適用上の注意
調製時
本剤は、抗ヒスタミン剤と混合すると反応し沈殿を生じるおそれがあるので、混注は避けること。
使用後
保存剤を添加していないので、残液を保存使用しないこと。
その他の注意
動物実験での反復投与試験(ラット)において高用量で対照薬(ヘパリン)に比べて軽度の骨多孔症がみられたとの報告がある。
外来透析患者では、穿刺部の止血を確認してから帰宅させること。
ヘパリン起因性血小板減少症(HIT)はヘパリン−血小板第4因子複合体に対する自己抗体(HIT抗体)の出現による免疫学的機序を介した病態であり、重篤な血栓症(脳梗塞、肺塞栓症、深部静脈血栓症等)を伴うことがある。HIT発現時に出現するHIT抗体は100日程度で消失〜低下するとの報告がある(「原則禁忌」の項参照)。また、投与終了数週間後に、HITが遅延して発現したとの報告もある。
本剤は未分画ヘパリンや他の低分子量ヘパリン又は合成多糖類と製造工程、分子量の分布が異なり、同一単位(抗第Xa因子活性)でも他のヘパリン類とは必ずしも互換性がないため、投与量の設定の際には本剤の用法・用量に従うこと。
薬効薬理
ダルテパリンナトリウムはアンチトロンビンIII(ATIII)と結合することにより、第Xa因子に対する阻害作用を促進する。1)
有効成分に関する理化学的知見
一般名
ダルテパリンナトリウム(Dalteparin Sodium)
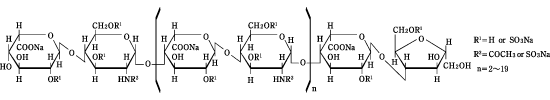
構造式
分子量
平均相対分子量約5,000
性状
本品は白色〜帯灰褐色の粉末又は塊で、においはなく、吸湿性である。
本品は水に溶けやすく、エタノール(99.5)にほとんど溶けない。
本質
ブタの小腸粘膜由来のヘパリンを亜硝酸分解して得た解重合ヘパリンのナトリウム塩;平均相対分子量は約5,000で、硫酸エステル化の度合は二糖当たり2〜2.5である。
取扱い上の注意
安定性試験
本剤を用いた加速試験(40℃、相対湿度75%、6ヵ月)の結果、ダルテパリンNa静注5千単位/5mL「HK」は通常の市場流通下において3年間安定であることが推測された2)。
包装
5mL(5,000低分子ヘパリン国際単位)×10瓶(ガラスバイアル)
主要文献及び文献請求先
主要文献
1
USP DI 25th ed.,Vol.I,1072(2005)
2
光製薬社内資料(安定性試験)
文献請求先
主要文献に記載の社内資料につきましても下記にご請求下さい。
光製薬株式会社 医薬情報部
〒111-0024 東京都台東区今戸2丁目11番15号
TEL 03-3874-9351
FAX 03-3871-2419
製造販売業者等の氏名又は名称及び住所
製造販売元
光製薬株式会社
東京都台東区今戸2丁目11番15号