作成又は改訂年月
**印:
2021年2月改訂
(第11版)
*印:
2017年12月改訂
日本標準商品分類番号
日本標準商品分類番号等
薬効分類名
承認等
販売名
スルプロチン軟膏1%
販売名コード
承認・許可番号
22000AMX02298000
SULPROTIN
薬価収載
販売開始
使用期限等
貯 法
しゃ光保存
使用期限
外装に表示の使用期限内に使用すること。
組成
1g中:スプロフェン………………10mg(1%)
〈添加物〉
白色ワセリン、流動パラフィン
性状
においのない白色〜微黄色半透明の軟膏
識別コード
SP-O
販売名
スルプロチンクリーム1%
販売名コード
承認・許可番号
22000AMX02299000
SULPROTIN
薬価収載
販売開始
使用期限等
貯 法
しゃ光保存
使用期限
外装に表示の使用期限内に使用すること。
組成
1g中:スプロフェン………………10mg(1%)
〈添加物〉
2-オクチルドデカノール、自己乳化型モノステアリン酸グリセリル、ジメチルポリシロキサン、スクワラン、セタノール、大豆レシチン、トコフェロール酢酸エステル、トリ(カプリル・カプリン酸)グリセリル、白色ワセリン、パラオキシ安息香酸ブチル、パラオキシ安息香酸メチル、プロピレングリコール、ポリオキシエチレンセチルエーテル、pH調節剤
性状
においはないか、又はわずかに特異なにおいを有する白色〜淡黄白色の乳剤性の軟膏
識別コード
SP-C
一般的名称
禁忌
本剤の成分に対し過敏症の既往歴のある患者
ケトプロフェン(外皮用剤)、チアプロフェン酸、フェノフィブラート及びオキシベンゾンに対して過敏症の既往歴のある患者[これら製剤との交叉感作性により、本剤の使用によって過敏症を誘発するおそれがある]
効能・効果
急性湿疹、接触皮膚炎、アトピー性皮膚炎、慢性湿疹、皮脂欠乏性湿疹、酒さ様皮膚炎・口囲皮膚炎、帯状疱疹
用法・用量
急性湿疹、接触皮膚炎、アトピー性皮膚炎、慢性湿疹、皮脂欠乏性湿疹、酒さ様皮膚炎・口囲皮膚炎
本品の適量を1日数回患部に塗布する。
帯状疱疹
本品の適量を1日1〜2回患部に塗布又は貼布する。
使用上の注意
重要な基本的注意
本剤の長期使用により過敏症状があらわれる可能性がある。
副作用
副作用等発現状況の概要
〈軟膏製剤〉
スプロフェンを1%含有する軟膏製剤における承認時及び使用成績調査の結果を集計したところ、安全性検討症例14,044例中副作用が報告されたのは、186例(1.32%)であり、主な副作用は発赤64件(0.46%)、刺激感57件(0.41%)、そう痒53件(0.38%)、紅斑44件(0.31%)等であった。また、臨床検査は112例に実施されたが、本剤に起因すると考えられる変化は認められなかった。(再審査終了時)
〈クリーム製剤〉
スプロフェンを1%含有するクリーム製剤における承認時及び使用成績調査の結果を集計したところ、安全性検討症例1,750例中副作用は56例(3.20%)であり、主な副作用は刺激感32件(1.83%)、発赤13件(0.74%)、そう痒10件(0.57%)、紅斑10件(0.57%)等であった。(再審査終了時)
その他の副作用
皮膚注)
0.1〜5%未満
刺激感、発赤、そう痒、腫脹、紅斑、丘疹、落屑、接触皮膚炎
皮膚注)
0.1%未満
光線過敏症
注)発現した場合は、使用を中止すること。
妊婦、産婦、授乳婦等への投与
**妊婦又は妊娠している可能性のある女性に対しては、治療上の有益性が危険性を上回ると判断される場合にのみ使用すること。[妊婦に対する安全性は確立していない]
**シクロオキシゲナーゼ阻害剤(経口剤、坐剤)を妊婦に使用し、胎児の腎機能障害及び尿量減少、それに伴う羊水過少症が起きたとの報告ある。
小児等への投与
低出生体重児、新生児又は乳児に対する長期投与の安全性は確立していない(使用経験が少ない)。
適用上の注意
使用時:大量又は広範囲の使用は避けること。
投与経路:眼科用に使用しないこと。
その他の注意
外国では経口投与において側腹部痛(急激な尿酸排泄による尿酸結石)が報告されており、日本及び外国で経口剤は発売されていない。
薬物動態
スプロフェン軟膏を20g(スプロフェンとして200mg)健康成人(5名)の背部皮膚にODT法により8時間塗布したときの血清及び尿中のスプロフェン及びその代謝産物を定量した。
血中濃度1)
スプロフェンは、塗布後約9.0時間で最高血中濃度(約0.21μg/mL)に達し、生物学的半減期は約3.1時間であった。
血中代謝産物は、スプロフェンとその抱合体及び2-[p-(α-ハイドロキシ-2-テニル)フェニル]プロピオン酸であり、スプロフェンの濃度が最も高かった。
尿中排泄1)
尿中にはスプロフェンとその代謝産物及びそれぞれの抱合体が排泄され、これらの総量は塗布後24時間までで塗布量の約6.2%であった。
(参考)2)3)
スプロフェン軟膏をラット正常皮膚に8時間密封塗布した結果、スプロフェンは代謝されることなく塗布部位の皮膚中に分布した。ラット損傷皮膚に塗布した場合、正常皮膚に比較し速やかに吸収され、血中濃度、塗布部位皮膚及び各種組織中濃度とも高かった。しかし、正常皮膚、損傷皮膚ともに皮膚内濃度に比較し血中濃度及び各種組織中濃度は著しく低いことが認められた。正常皮膚に塗布したときの尿糞中排泄率は塗布量に対してラットで約23%、モルモットで約11%であった。また連続投与による蓄積性は認められなかった。
臨床成績
スプロフェンを1%含有する軟膏製剤及びクリーム製剤における承認時までの比較試験を含む臨床試験及び使用成績調査における成績の概要は次のとおりであった。4)〜14)
| 疾患名\改善度 | 改善症例数/症例数(%)
軟 膏 | 改善症例数/症例数(%)
クリーム |
| 急性湿疹 | 1,549/1,887(82.1) | 261/320(81.6) |
| 接触皮膚炎 | 910/1,132(80.4) | 162/204(79.4) |
| アトピー性皮膚炎 | 1,592/2,709(58.8) | 158/283(55.8) |
| 慢性湿疹 | 700/1,045 (67.0) | 130/219(59.4) |
| 皮脂欠乏性湿疹 | 1,586/2,047(77.5) | 163/208(78.4) |
| 酒さ様・口囲皮膚炎 | 458/705 (65.0) | 61/90 (67.8) |
| 帯状疱疹 | 2,740/3,056(89.7) | 189/215(87.9) |
| 合 計 | 9,535/12,581(75.8) | 1,124/1,539(73.0) |
薬効薬理
抗炎症作用15)
ラットにおける血管透過性亢進抑制作用、カラゲニン足蹠浮腫抑制作用、肉芽増殖抑制作用、モルモットにおける紫外線紅斑抑制作用等の抗炎症作用が認められた。
鎮痛作用15)
ラットの炎症性疼痛に対し、疼痛閾値を上昇させ、著明な鎮痛作用が認められた。
作用機序
スプロフェンにはプロスタグランジン生合成阻害作用が認められており、これに基づいて種々の抗炎症作用を示すと考えられる。
有効成分に関する理化学的知見
一般名
スプロフェン(Suprofen)
化学名
(±)-2-[p-(2-Thenoyl)phenyl]propionic acid
分子式
C14H12O3S
分子量
260.31
融 点
124〜127℃
性 状
白色〜帯黄白色の結晶性の粉末である。メタノール、エタノール(99.5)、アセトン又は1,4-ジオキサンに溶けやすく、水に極めて溶けにくい。水酸化ナトリウム試液又はアンモニア試液に溶ける。1,4-ジオキサン溶液(1→40)は旋光性を示さない。
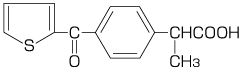
構造式
取扱い上の注意
安定性試験結果の概要16)
●スルプロチン軟膏1%
長期保存試験(4年)の結果、スルプロチン軟膏1%は通常の市場流通下において4年間安定であることが確認された。
●スルプロチンクリーム1%
加速試験(40℃、相対湿度75%、6ヵ月)の結果、スルプロチンクリーム1%は通常の市場流通下において3年間安定であることが推測された。
包 装
*●スルプロチン軟膏1%
10g×10
●スルプロチンクリーム1%
10g×10
主要文献
1
東等:薬理と治療,15(10),4041,1987
2
横家等:ibid.,15(10),4009,1987
3
横家等:ibid.,15(10),4023,1987
4
原田等:臨床医薬,3(10),1187,1987
5
原田等:ibid.,3(10),1197,1987
6
原田等:ibid.,3(10),1209,1987
7
原田等:ibid.,3(10),1229,1987
8
大河原等:ibid.,3(10),1239,1987
9
石橋等:ibid.,3(10),1255,1987
10
中溝等:薬理と治療,15(10),4315,1987
11
朝田等:ibid.,15(11),4899,1987
12
坂井等:ibid.,15(11),4911,1987
13
植木等:ibid.,15(11),4919,1987
14
原田等:ibid.,19(10),4287,1991
15
久木等:ibid.,15(9),3631,1987
16
武田テバファーマ(株)社内資料(安定性試験)
文献請求先・製品情報お問い合わせ先
主要文献欄に記載の文献・社内資料は下記にご請求下さい。
武田テバファーマ株式会社 武田テバDIセンター
〒453-0801 名古屋市中村区太閤一丁目24番11号
TEL 0120-923-093
受付時間 9:00〜17:30(土日祝日・弊社休業日を除く)
製造販売業者等の氏名又は名称及び住所
販売
武田薬品工業株式会社
大阪市中央区道修町四丁目1番1号
製造販売元
武田テバファーマ株式会社
名古屋市中村区太閤一丁目24番11号