1
中島嘉助 他:日本歯科評論 1974;384:168-174
2
黒須義宇 他:基礎と臨床 1984;18(3):903-908
3
第十八改正日本薬局方解説書. 2021:C3305-3313
4
社内資料:生物学的同等性試験
口腔粘膜治療剤
1g 45円
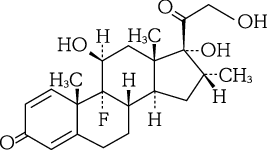
有効成分 | 1g中 日局 デキサメタゾン 1mg |
|---|---|
添加剤 | 流動パラフィン、ヒドロキシプロピルセルロース、カルボキシビニルポリマー、ゲル化炭化水素 |
| 識別コード | CH-AK |
|---|---|
| 色調・剤形 | 白色~帯黄白色のなめらかな軟膏剤である。 |
頻度不明 | |
|---|---|
口腔の感染症注1) | 口腔の真菌性及び細菌性感染症 |
過敏症 | 過敏症 |
下垂体・副腎皮質系機能注2) | 下垂体・副腎皮質系機能の抑制 |