1
厚生労働省健康局結核感染症課編:抗微生物薬適正使用の手引き
2
山作房之輔:臨床成人病. 1976;6(1):95-104
3
山作房之輔ほか:Chemotherapy. 1981;29(12):1393-1400
4
吉田眞一ほか:戸田新細菌学. 2010;33 版:165-167、㈱南山堂
5
中沢昭三ほか:Chemotherapy. 1974;22(5):779-785
アミノグリコシド系抗生物質製剤
1瓶 580円
| 有効成分 | 1バイアル中日局ジベカシン硫酸塩100mg(力価) |
|---|
| 形状 | 塊又は粉末(凍結乾燥品) |
|---|---|
| 色 | 白色~黄白色 |
| pH | 6.0~8.0 [50mg(力価)/mL溶液] |
| 浸透圧比 (日局生理食塩液対比) | 約0.5 [50mg(力価)/mL水溶液] |
障害度 | 初回量 | 投与間隔(時間) |
30>Ccr>10 10>Ccr | 50mg※ 50mg※ | 12~24 24~48 |
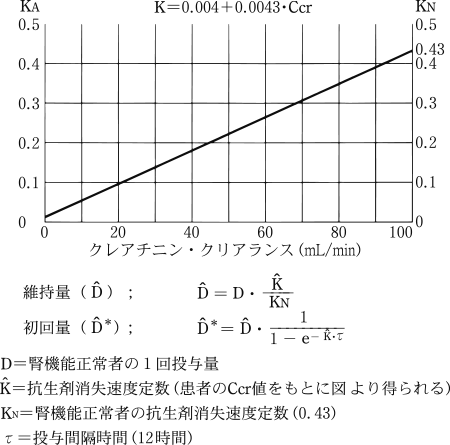
| 薬剤名等 | 臨床症状・措置方法 | 機序・危険因子 |
|---|---|---|
腎障害を起こすおそれのある血液代用剤 デキストラン ヒドロキシエチルデンプン等 | 腎障害が発現、悪化することがあるので、併用は避けることが望ましい。 腎障害が発生した場合には、投与を中止し、透析療法等適切な処置を行うこと。 | 機序は明確ではないが、併用によりアミノグリコシド系抗生物質の血中への蓄積、近位尿細管上皮の空胞変性が生じるという報告がある。 |
ループ利尿剤 フロセミド アゾセミド等 | 腎障害及び聴器障害が発現、悪化するおそれがあるので、併用は避けることが望ましい。 | 機序は明確ではないが、併用によりアミノグリコシド系抗生物質の血中濃度の上昇、腎への蓄積が起こるという報告がある。 |
腎毒性及び聴器毒性を有する薬剤 バンコマイシン塩酸塩 エンビオマイシン硫酸塩 白金含有抗悪性腫瘍剤(シスプラチン、カルボプラチン、ネダプラチン)等 | 腎障害及び聴器障害が発現、悪化するおそれがあるので、併用は避けることが望ましい。 | 両薬剤ともに腎毒性、聴器毒性を有するが相互作用の機序は不明。 |
麻酔剤 筋弛緩剤 ベクロニウム臭化物 A型ボツリヌス毒素等 | 呼吸抑制があらわれるおそれがある。 呼吸抑制があらわれた場合には、必要に応じ、コリンエステラーゼ阻害剤、カルシウム製剤の投与等の適切な処置を行うこと。 | 両薬剤ともに神経筋遮断作用を有しており、併用によりその作用が増強される。 |
腎毒性を有する薬剤 シクロスポリン アムホテリシンB等 | 腎障害が発現、悪化するおそれがある。 | 両薬剤ともに腎毒性を有するが、相互作用の機序は不明。 |
0.1~5%未満 | 0.1%未満 | |
|---|---|---|
過敏症 | 発疹 | 紅斑、浮腫性紅斑、瘙痒、発熱 |
腎臓 | BUN、クレアチニンの上昇 | 浮腫、蛋白尿、血尿、カリウム等電解質の異常 |
肝臓 | AST、ALT、Al-P、LDHの上昇 | |
消化器 | 下痢 | 悪心・嘔吐、食欲不振 |
血液 | 貧血、好酸球増多 | |
ビタミン欠乏症 | ビタミンK欠乏症状(低プロトロンビン血症、出血傾向等)、ビタミンB群欠乏症状(舌炎、口内炎、食欲不振、神経炎等) | |
注射部位 | 注射局所の疼痛又は硬結(筋肉内注射時) | |
その他 | 頭痛、口唇部のしびれ感 |
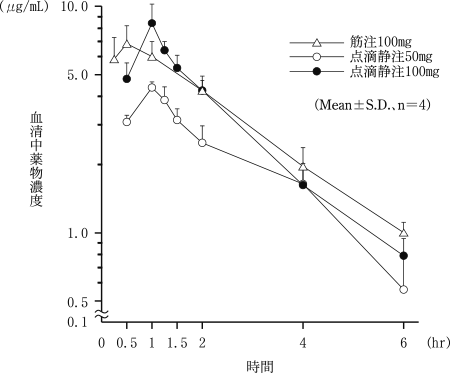
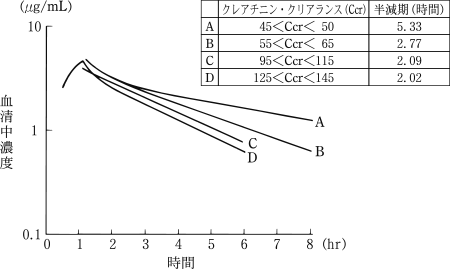
被験菌 | MIC(μg/mL) |
Staphylococcus aureus 209-P JC | 0.05 |
Escherichia coli NIH JC | 1.56 |
Klebsiella pneumoniae | 0.2 |
Proteus vulgaris OX-19 | 1.56 |
Proteus mirabilis 1287 | 3.12 |
Proteus morganii Kono | 1.56 |
Pseudomonas aeruginosa No.12 | 0.78 |
Pseudomonas aeruginosa ATCC 10145 | 1.56 |